
Rappresentazione in 3D di vertebre con osteoporosi (illustrazione).
L '= L'Arsenale terapeutico dell'osteoporosi è arricchito con un nuovo farmaco basato su Tériparatide, TERROSA 20 µg/80 µL di soluzione iniettabile in cartuccia, indicato negli adulti, in:
- Il trattamento dell'osteoporosi nei pazienti ad alto rischio di frattura: osteoporosi postmenopausica e osteoporosi maschile. Nelle donne in menopausa è stata dimostrata una riduzione significativa dell'incidenza di fratture vertebrali e periferiche, ma non fratture dell'anca ( CF. vidal Reco "Osteoporosi");
- Il trattamento dell'osteoporosi corisonica nelle donne e negli uomini ad alto rischio di frattura che riceve una terapia corticosteroide a lungo termine. Europeo.
TERROSA a reçu une autorisation de mise sur le marché (AMM) européenne.
= È soggetto a monitoraggio aggiuntivo che consentirà la rapida identificazione di nuove informazioni relative alla sicurezza. Gli operatori sanitari dichiarano qualsiasi effetto sospetto indesiderabile.
Secondo Biosimilaire di Forsteo disponibile in Italia
== Terrosa è il secondo biosimilaire di FORSTEO 20 µg/80 µl di soluzione iniettabile in penna pre -riempita reso disponibile in Italia, dopo Movymia 20 µg/80 µL Soluzione iniettabile CARTOUCHE ( CF.notre article du 7 octobre 2019, actualisé le 15 avril et 2 octobre 2020).
come la sua medicina di riferimento, Terrosa è formulata da Tériparatide (20 µg/80 µL), prodotto su Escherichia coli dalla tecnica del DNA ricombinante.
L'AMM europeo è stato concesso a Terrosa sulla base di uno studio sull'equivalenza farmacocinetica tra Terrosa e Forsteo (cfr. Parere della Commissione di trasparenza del 15 aprile 2020).
Aucune étude d'équivalence clinique n'a été fournie.
Due presentazioni: una per l'inizio del trattamento, l'altro per i rinnovi
Sono proposte due presentazioni Terrosa:
- in una scatola di 1 cartuccia fornita con 1 Pen Pen Terosa, per consegnare l'inizio del trattamento;
- in scatola di solo 1 cartuccia, da favorire per i rinnovi del trattamento.
Terosa in cartuccia deve essere usato solo con la penna Terrosa.
Terosa in pratica: dosaggio e manipolazione della penna Terrosa
= Il dosaggio raccomandato di Terrosa è di 20 µg 1 volta al giorno, per iniezione sottocutanea (SC).
= I siti di iniezione raccomandati sono coscia e addome. Un nuovo ago deve essere utilizzato ad ogni iniezione.
I pazienti devono essere integrati con calcio e vitamina D se l'assunzione di cibo è insufficiente.
= La durata totale massima del trattamento con il tériparatide fornito dall'AMM deve essere di 24 mesi (18 mesi secondo le raccomandazioni di Has). Questo trattamento di 24 mesi da parte di Tériparatide non deve essere rinnovato durante la vita di un paziente. Altri trattamenti di osteoporosi possono essere utilizzati dai pazienti dopo l'interruzione del trattamento con tériparatide.
Descrizione della penna Terrosa
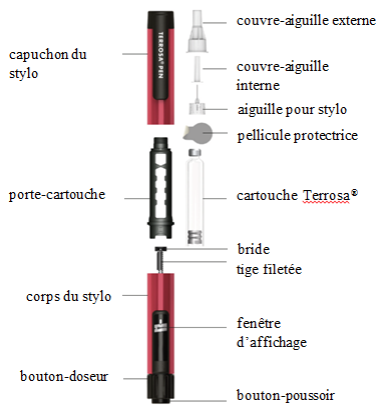 La Pen Pen Terosa è un sistema di somministrazione multidosi riutilizzabile. È composto da 3 parti:
La Pen Pen Terosa è un sistema di somministrazione multidosi riutilizzabile. È composto da 3 parti:
- il cappuccio, che protegge il supporto di carota;
- il vettore di carota, in cui la cartuccia deve essere inserita;
- il corpo della penna, con una finestra di visualizzazione, e si è concluso con il pulsante Doser e il pulsante PIMM. | Dose da iniettare, espressa in microlitri (80 µl per iniezione). Questo pulsante Doser è bloccato se la quantità rimanente nella cartuccia è inferiore a 80 µL.
Per ogni iniezione, deve essere utilizzato un nuovo ago ( CF. incorniciata 1). Gli aghi non sono forniti nel kit Terosa.
Terrosa Pen è l'unica penna adatta all'iniezione di Terrosa.
incorniciata 1 - aghi compatibili con la penna per la penna Terrosa
|
Supporto per i pazienti: iniezione, tracciabilità e conservazione
= I pazienti devono essere addestrati in iniezione di SC con la Penna Terrosa.
= Inoltre, le istruzioni per la sicurezza e la conservazione devono essere sottolineate:
- Registra la data della prima iniezione sulla scatola di Terrosa, nello spazio "primo uso" fornito a questo scopo;
- Nota il numero batch e la prima data di iniezione di ciascuna cartuccia, su un calendario;
- prima dell'uso, mantieni la terrosa in frigorifero, tra 2 e 8 ° C;
- une fois la cartouche insérée dans le stylo, l'ensemble cartouche/stylo doit être remis au réfrigérateur après chaque utilisation et utilisé dans un délai maximal de 28 jours (d'où l'importance d'inscrire la date de première utilisation sur la boîte de TERROSA) ;
- changer d'aiguille à chaque injection.
Identità amministrativa
- elenco I
- Box di 1 cartuccia, CIP 34009 3019820 9
- = Box di 1 cartuccia e 1 Penna Terosa, CIP 34009 3019822 3
- rimborsabile al 65 % in base alla procedura di farmaci eccezionali (foglio di informazioni terapeutiche - Journal ufficiale del 24 novembre 2020 - Testo 17) | 232,71 euro (per le due presentazioni)
- Prix public TTC = 232,71 euros (pour les deux présentations)
- Approvazione alle comunità ( Journal ufficiale del 24 novembre - Testo 18)
- rimborso limitato a 18 mesi di trattamento
- Scarico al gruppo Tériparatide su | Biologici simililiste de référence des groupes biologiques similaires (ANSM, 18 agosto 2020)
- Freccia di laboratorio generici
incorniciata 2 - Perimetro di rimborso Terrosa
|
Pour aller plus loin
Avis de la Commission de la Transparence - TERROSA (ha, 15 aprile 2020)
=
per andare oltre
Consultare le monografie vidali
Fonti
per ricevere tutte le notizie via e -mail gratuitamente I sottoscrizione!

 4 minuti
4 minuti Aggiungi un commento
Aggiungi un commento

Commenti
Clicca qui per tornare alla reception.