Achondroplasia è dovuta a una mutazione del gene FGFR3 situato a livello del cromosoma 4.
Voxzogo in polvere e solvant per la soluzione iniettabile è un nuovo farmaco indicato nel trattamento dell'acidroplasia, di età pari o superiore alle cui epifisi non sono unite. La diagnosi di achondroplasia deve essere confermata da uno screening genetico appropriato.
Voxzogo è formulato da un nuovo ingrediente attivo, il Vosoritide. È proposto in tre dosaggi: 0,4 mg, 0,56 mg e 1,2 mg.
VOXZOGO est le premier médicament à disposer d'une autorisation de mise sur le marché (AMM) dans le traitement de cette maladie génétique rare ; il a le statut de médicament orphelin. La Commission de la transparence (CT) lui a attribué un service médical rendu (SMR) important et une amélioration du service médical rendu modérée (ASMR III) par rapport à la stratégie thérapeutique actuelle (traitement préventif et symptomatique).
Voxzogo è un trattamento giornaliero, nell'iniezione sottocutanea (SC). La soluzione di iniezione deve essere ricostruita dalla polvere e dal solvente fornito (acqua per preparazione iniettabile).
Le singole siringhe presenti nella scatola devono essere utilizzate per prendere e iniettare la soluzione iniettabile.
La dose abituale è di 15 µg/kg di peso corporeo. La dose e il volume da iniettare devono essere regolarmente regolati in base al peso, quindi la necessità di un regolare monitoraggio della crescita.
Pour réduire les manifestations d'une éventuelle diminution de la pression artérielle après l'injection, il est recommandé aux patients de prendre un repas léger et de boire un verre de liquide environ 30 minutes avant l'injection.
Voxzogo è disponibile in città e in ospedale. In città, il tasso di rimborso è fissato al 65 %. Qualunque sia il dosaggio, la base di rimborso è di 7.406,41 euro tra cui tasse (scatola di 10 bottiglie, 10 siringhe solventi, 10 siringhe vuote e 10 aghi).
La prescrizione di Voxzogo è ospedale e limitato.
L una polvere di voxzogo specializzata e solvente indicati nel trattamento di Achondroplasia in pazienti di età pari o superiore a 2 anni e le cui epifisi non sono saldate. La diagnosi di achondroplasia deve essere confermata da uno screening genetico appropriato.
Voxzogo contiene un nuovo ingrediente attivo, il Vosoritide ( CF. incorniciata). | :
VOXZOGO est mis à disposition en ville et à l'hôpital, sous trois dosages :
- Voxzogo 0,4 mg di polvere e solvente per soluzione iniettabile, la cui bottiglia di polvere è riconoscibile da un opercolo bianco;
- Voxzogo 0,56 mg di polvere e solvente per soluzione iniettabile, la cui bottiglia di polvere è riconoscibile da una loggia magenta; | e solvente per soluzione di iniezione, la cui bottiglia in polvere è riconoscibile da un grigio coperte.
- VOXZOGO 1,2 mg poudre et solvant pour solution injectable, dont le flacon de poudre est reconnaissable par un opercule gris.
|
Il Vosoritide è un peptide natriuretico di tipo C modificato (CNP). Nei pazienti con burnoplasia, la crescita ossea endocondrale è regolata negativamente a causa della mutazione del ricevitore 3 del fattore di crescita fibroblastico (FGFR3). Il collegamento del tiritide al ricevitore B dei peptidi natriuretici (NPR-b) antagonizzato dell'FGFR3 inibendo le chinasi 1 e 2 regolate da segnali extracellulari (ERK1/2) nel percorso della chinasi della mappa (MAPK)rapidly accelerating fibrosarcoma, fibrosarcome à accélération rapide). Di conseguenza, il Vosoritide, come CNP, funge da regolatore positivo della crescita ossea endocondrale, perché promuove la proliferazione e la differenziazione dei condrociti. |
Voxzogo è oggetto di monitoraggio aggiuntivo che consentirà la rapida identificazione di nuove informazioni relative alla sicurezza. Gli operatori sanitari dichiarano qualsiasi sospetto effetto avverso.
Un premier médicament pour traiter l'achondroplasie
Achondroplasia è una forma di displasia ossea, la forma più frequente di questa malattia rara. È di origine genetica e risulta da una mutazione del gene FGFR3 ( Fibroblast Fattore di crescita Recettore Tipo 3). Questa mutazione porta a una produzione eccessiva della proteina FGFR3 e accentua la sua azione regolatoria negativa sulla crescita ossea longitudinale. Nelle persone con questa mutazione, è influenzata la crescita ossea del cranio, della colonna vertebrale, delle braccia e delle gambe.
Voxzogo è il primo farmaco con un'indicazione nel trattamento dell'acidroplasia. L'attuale gestione si basa essenzialmente sulle cure di supporto, con scopi preventivi e sintomatici (trattamento delle complicanze della malattia).
come trattamento per una malattia rara (da 3,72 a 4,6 per 100.000 nascite), il voxzogo è considerato un farmaco orfano. Il numero di pazienti in Italia che probabilmente trarrà beneficio da questo trattamento è stimato tra 360 e 620 [ 1].
Avant de recevoir son autorisation de mise sur le marché (AMM), VOXZOGO a bénéficié en France d'une autorisation temporaire d'utilisation (ATU) de cohorte dès juin 2021, chez les patients âgés de 5 ans et plus.
Évaluation médico-économique : une ASMR de niveau III par rapport à la prise en charge actuelle
nella sua opinione del 15 dicembre 2021 [ 1], la Commissione di trasparenza (CT) attribuita a Voxzogo:
- Un servizio medico reso (SMR) importante;
- Un miglioramento del servizio medico reso moderato (ASMR III) rispetto alla gestione attuale, essenzialmente basata su cure di supporto volta alla prevenzione e al trattamento delle molteplici complicanze della malattia.
Il CT si basa principalmente sui risultati di due studi comparativi controllati contro Placebo, randomizzato, in doppio cieco, effettuato in pazienti con achondroplasia geneticamente confermata:
- Uno studio di fase III (111-301 [ 2] avendo incluso bambini dai 5 ai 18 anni (n = 121) e lo studio di estensione in un aprile non comparativo (111-302): valutazione dell'efficacia dell'efficacia della volto sulla crescita a 52 settimane, in termini di variazione non comparativa; Studio di follow-up aperto non comparativo: valutazione dell'efficienza dell'orientamento sulla crescita e la sua tolleranza a 52 settimane, in termini di variazione del punteggio Z di dimensioni/lunghezza rispetto all'inclusione. Achondroplasia.
- étude de phase II ayant inclus des nourrissons et des enfants âgés de moins de 5 ans, et l'étude de suivi en ouvert non comparative : évaluation de l'efficacité du vosoritide sur la croissance et sa tolérance à 52 semaines, en termes de variation du Z-score de la taille/longueur par rapport à l'inclusion. Les données disponibles n'ont concerné que 4 enfants âgés de 2 à 5 ans.
La CT a également pris en compte une étude observationnelle multicentrique et internationale évaluant l'intérêt de VOXZOGO sur la croissance des patients pédiatriques atteints d'achondroplasie.
Selon les résultats de l’étude randomisée en double aveugle menée chez les enfants âgés de plus de 5 ans, la supériorité du vosoritide a été démontrée par rapport au placebo en termes de gain statural annuel, critère de jugement principal cliniquement pertinent selon la CT, avec une quantité d’effet également considérée comme cliniquement pertinente (+1,57 cm/an).
La CT note par ailleurs qu'il n'existe pas de comparateur médicamenteux cliniquement pertinent. VOXZOGO est le premier médicament pour traiter l'achondroplasie.
Dans la stratégie thérapeutique de l'achondroplasie, VOXZOGO est un traitement de première intention chez les patients âgés de 2 ans et plus dont les épiphyses ne sont pas soudées (croissance non terminée). Il doit être instauré le plus précocement possible et doit être arrêté dès que la croissance est achevée.
Voxzogo in pratica
Voxzogo si presenta in una bottiglia di polvere da ricostruire con il solvente fornito nella siringa pre -riempita (acqua per preparazione iniettabile).
ogni casella di Voxzogo contiene:
- 10 flacons de poudre ;
- 10 seringues préremplies d'eau pour préparation injectable (solvant) ;
- 10 aghi per uso singolo per la ricostruzione (da fissare sulla siringa del solvente); | Con ago (per iniezione).
- 10 seringues individuelles à usage unique avec aiguille (pour l'injection).
Dopo la ricostruzione, le concentrazioni delle soluzioni iniettabili ottenute sono le seguenti:
- per la specialità Voxzogo 0,4 mg: 0,8 mg/ml;
- per la specialità Voxzogo 0,56 mg: 0,8 mg/mL; | La specialità Voxzogo 1,2 mg: 2 mg/ml.
- pour la spécialité VOXZOGO 1,2 mg : 2 mg/mL.
prima della ricostruzione, Voxzogo mantiene in frigorifero, tra 2 e 8 ° C.
Una conservazione a una temperatura ambiente inferiore a 30 ° C è possibile per un singolo periodo di massima 90 giorni (senza superare la data di scadenza). Oltre a questo periodo, il voxzogo dovrebbe essere usato e non dovrebbe essere somministrato al frigorifero.
Iniezione sottocutanea giornaliera
Il trattamento deve essere stabilito e seguito da un medico specializzato nella gestione dei disturbi della crescita o della displasia scheletrica.
È importante iniziare il trattamento nei bambini fin dalla tenera età.
Il trattamento con Voxzogo corrisponde a un'iniezione sottocutanea giornaliera (SC), se possibile contemporaneamente ogni giorno.
I siti di iniezione raccomandati sono le cosce, l'addome, la parte superiore dei glutei o la parte posteriore del braccio verso l'alta. Il voxzogo non deve essere iniettato nella stessa area di iniezione di 2 giorni di fila.
La soluzione iniettabile deve essere somministrata entro 3 ore dalla ricostruzione.
L'iniezione può essere effettuata da un caregiver addestrato nella ricostruzione e nell'iniezione di voxzogo. Solo la singola siringa fornita nella casella deve essere utilizzata per prendere il volume della soluzione iniettabile per somministrare e iniettarla.
Guarda il peso per regolare la dose
La dose abituale è di 15 µg/kg di peso corporeo. | peso. Si raccomanda un controllo sul peso, sulla crescita e sullo sviluppo fisico dei pazienti ogni 3-6 mesi.
Cette dose doit être réévaluée régulièrement et ajustée en fonction de la prise de poids. Un contrôle portant sur le poids, la croissance et le développement physique des patients est recommandé tous les 3 à 6 mois.
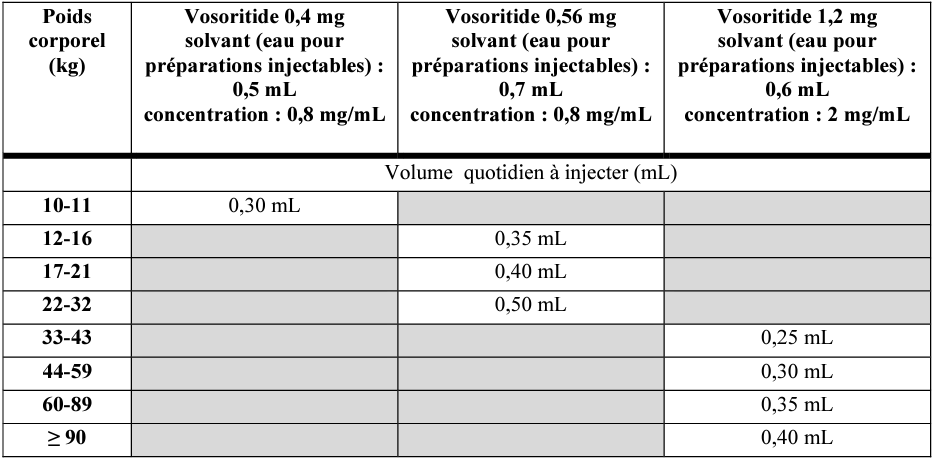
Il volume da gestire tiene conto di questa dose e la concentrazione della tua registrazione nella soluzione ricostituita ( CF. Tabella sotto).
Tabella - Volumi di prese uniche per peso corporeo [ 3]
Istruzioni per i pazienti: idratazione e pressione sanguigna
Voxzogo si espone a riduzioni transitorie di transizione, nel tempo che segue. I pazienti (o caregiver) devono sapere come riconoscere le manifestazioni di questo effetto indesiderato, vale a dire vertigini, affaticamento e vomito.
I pazienti devono essere ben idratati al momento dell'iniezione. Prendendo un pasto leggero o un drink (acqua, latte, succo, ecc.) Circa 30 minuti prima dell'iniezione riduce i segni e i sintomi di una possibile diminuzione della pressione sanguigna.
Identità amministrativa
elenco I
Prescrizione ospedaliera
=
Prescrizione iniziale e rinnovamento riservato agli specialisti in pediatria, endocrinologia, reumatologia o genetica medica
Sorveglianza speciale durante il trattamento
=
Voxzogo 0,4 mg, scatola di 10 bottiglie di polvere + 10 siringhe predefinite di solvente (0,5 ml) + 10 aghi + 10 siringhe, CIP 34009 3023667 3
=
Voxzogo 0,56 mg, scatola di 10 bottiglie di polvere + 10 siringhe predefinite con solvente (0,7 ml) + 10 aghi + 10 siringhe, CIP 34009 3023669 7
=
Voxzogo 1,2 mg, scatola di 10 bottiglie di polvere + 10 siringhe predefinite di solvente (0,6 ml) + 10 aghi + 10 siringhe, CIP 34009 3023670 3
=
Rimborsabile al 65 % [ 4]
=
Prezzo pubblico TTC = 7 406.41 Euro [ 5]
=
Approvazione per le comunità [ 6]
=
Biomarin Laboratory
[1] Opinione della Commissione di trasparenza - Voxzogo (ha, 15 dicembre 2021)
[3] Riepilogo delle caratteristiche del prodotto di Voxzogo (sul sito web EMA)
[4] Decreto del 7 dicembre 2022 Modifica dell'elenco delle specialità farmaceutiche. Voxzogo ( Journal ufficiale del 13 dicembre 2022 - Testo 48)
[5] recensioni relative ai prezzi di Voxzogo ( Journal ufficialedu 13 décembre 2022 - texte 123)
[6] Decreto del 7 dicembre 2022 Modifica dell'elenco delle specialità farmaceutiche approvate per l'uso di comunità e vari servizi pubblici - Voxzogo (= Journal ufficiale del 13 dicembre 2023-49) || 558

 8 minuti
8 minuti Aggiungi un commento
Aggiungi un commento

Commentaires
Clicca qui per tornare alla reception.