Inserisci almeno 3 caratteri per la tua ricerca.
- droghe
- Atectura Breezhaler
- Atectura Breezhal 125 µg/127,5 µg gel
Riepilogo
enveloppe de la gélule : gelatina
Inchiostro di stampa: Shellac,= biossido di titanio,= Ossido nero, propileneglycol,fer jaune oxyde,= idrossido di ammonio
een senza soglia di dose:= lattosio monoidrato
CIP: 340093020772
Metodi di ricerca: Prima di aprire: <30 ° per 36 mesi (Keep in the Shelter of Light, Keep nella sua confezione, Keep on Humidità)
CIP: 3400930207758
= Il rifugio della luce, mantienilo nella sua confezione, mantieni il rifugio dell'umidità)
forme e presentazioni |
Ateuctura 125 microgrammi/62,5 polvere di polvere per inalazione in capsule
polvere per inalazione (bianco) in capsula (trasparente, trasportando il codice del prodotto "IM150-80" stampato in blu sopra una linea blu sul corpo della capsula e il logo del prodotto stampato in blu e circondato da due linee blu sul tappo). | 30 x 1 capsule, sotto piastrine unità pre -taglio di 10, con 1 inalatore.
Boîte de 30 x 1 gélules, sous plaquettes prédécoupées unitaires de 10, avec 1 inhalateur.
10 x 1 capsule, sotto brochure unitaria pre -accoppiata, con 1 inalatore (modello ospedaliero).
= Atectura Breezhaler 125 microgrammi/127,5 microgrammi in polvere per inalazione nelle capsule | Inalazione (bianca) in capsula (trasparente, con il codice del prodotto "IM150-160" stampato in grigio sul corpo della capsula e il logo del prodotto stampato in grigio sul cappuccio).
Poudre pour inhalation (blanche) en gélule (transparente, portant le code produit « IM150-160 » imprimé en gris sur le corps de la gélule et le logo du produit imprimé en gris sur la coiffe).
10 x 1 capsule, sotto piastrine unitarie pre-tagliate di 10, con 1 inalatore.
10 x 1 unità capsule, con 1 inalatore (modello ospedaliero).
atectura breezhaler 125 microgrammi/260 microgrammi in polvere per inalazione in capsule
polvere per inalazione (bianco) in capsula (trasparente, trasportando il codice del prodotto "IM150-320" stampato in nero sopra due linee nere sul corpo della capsula e del prodotto stampato in nero e circondato da due linee nere sul copricapo).
= scatola di 30 x 1 capsule, sotto piastrine unità pre -taglio di 10, con 1 inalatore.
10 x 1 capsule, sotto una piastra pre -taglio unitaria, con 1 inalatore (modello ospedaliero). | Breezhaler 125 microgrammi/62,5 microgrammi in polvere per inalazione in capsule
COMPOSITION |
Atectura Breezhaler 125 microgrammes/62,5 microgrammes poudre pour inhalation en gélules
Ogni capsula contiene 150 mcg di indecaterolo (sotto forma di acetato) e 80 mcg di Mometasone furoato. | INDACATEROL (sotto forma di acetato) e 62,5 mcg di Mometasone furoato.
Chaque dose délivrée à la sortie de l'embout buccal de l'inhalateur contient 125 mcg d'indacatérol (sous forme d'acétate) et 62,5 mcg de furoate de mométasone.
atectura breezhaler 125 microgrammi/127,5 microgrammi in polvere per inalazione nelle capsule
Chaque gélule contient 150 mcg d'indacatérol (sous forme d'acétate) et 160 mcg de furoate de mométasone.
Chaque dose délivrée à la sortie de l'embout buccal de l'inhalateur contient 125 mcg d'indacatérol (sous forme d'acétate) et 127,5 mcg de furoate de mométasone.
Atectura Breezhaler 125 microgrammes/260 microgrammes poudre pour inhalation en gélules
Chaque gélule contient 150 mcg d'indacatérol (sous forme d'acétate) et 320 mcg de furoate de mométasone.
Chaque dose délivrée à la sortie de l'embout buccal de l'inhalateur contient 125 mcg d'indacatérol (sous forme d'acétate) et 260 mcg de furoate de mométasone.
Ordine con un effetto noto:
Ogni capsula contiene circa 24 mg di lattosio (monoidrato).
= Contenuto della capsula: lattosio monoidrato.
Inviluppo della capsula: gelatina.
Printing Ench:
= Atectura Breezhaler 125 microgrammi/62,5 microgrammi in polvere per inalazione nelle capsule: Shellac, Brilliant Blue FCF (E133), propilen glicole (E1520), biossido di titanio (E171), ossido di ferro (E172).
atectura breezhaler 125 microgrammi/127,5 microgrammi in polvere per inalazione nelle capsule: Shellac, biossido di titanio (E171), ossido di ferro nero (E172), propilenico glicole (E1520), ossido giallo (E172), idrossido di ammonio (E527).
atectura breezhaler 125 microgrammi/260 microgrammi in polvere per inalazione nelle capsule: S Hellac, ossido di ferro nero (E172), glicole propilenico (E1520), idrossido di ammonio (E527).
Indicazioni |
Atectura breezhaler è indicato nel trattamento continuo dell'asma negli adulti e negli adolescenti di età compresa tra 12 anni e più insufficientemente controllato dalla presa di un corticosteroide inalato e una beta-2-agonista di a breve termine illegale. | Amministrazione
POSOLOGIE ET MODE D'ADMINISTRATION |
Connettiti per accedere a questo contenuto
Contraindicazioni |
Connect per accedere a questo contenuto
caldi e precauzioni per l'uso |
= per il trattamento dei sintomi acuti dell'asma, inclusi episodi acuti di broncospasmo. In queste situazioni è consigliabile utilizzare un broncodilatatore a breve termine. Un aumento del consumo di broncodilatatori a breve durata per alleviare i sintomi indica un deterioramento del controllo dell'asma e i pazienti devono consultare un medico.
Ce médicament ne devrait pas être utilisé pour le traitement des symptômes aigus de l'asthme, y compris les épisodes aigus de bronchospasme. Dans ces situations il convient d'avoir recours à un bronchodilatateur de courte durée d'action. Une augmentation de la consommation de bronchodilatateurs de courte durée d'action pour soulager les symptômes indique une détérioration du contrôle de l'asthme et les patients doivent consulter un médecin.
I pazienti non devono interrompere il trattamento senza richiedere il consiglio di un medico, i sintomi potrebbero riapparire quando si smette il trattamento. | Questo farmaco. Se i pazienti non sentono un'efficacia del loro trattamento, non dovrebbero interromperlo ma consultare un medico. L'aumento del consumo di broncodilatatori di salvataggio indica un aggravamento dell'asma che giustifica una rivalutazione del trattamento. Un deterioramento improvviso e progressivo dei sintomi dell'asma può potenzialmente iniziare la prognosi vitale e richiedere una consulenza medica di emergenza.
Il est recommandé de ne pas arrêter brutalement le traitement par ce médicament. Si les patients ne ressentent pas une efficacité de leur traitement, ils ne doivent pas l'interrompre mais consulter un médecin. L'augmentation de la consommation de bronchodilatateurs de secours indique une aggravation de l'asthme qui justifie une réévaluation du traitement. Une détérioration soudaine et progressive des symptômes de l'asthme peut potentiellement engager le pronostic vital et nécessiter une consultation médicale en urgence.
Ipersensibilità
sono state osservate reazioni di ipersensibilità immediata dopo la somministrazione di questo farmaco. In caso di comparsa di segni evocativi di reazioni allergiche, in particolare un angiœdema (comprese le difficoltà respiratorie, i disturbi della deglutizione, il gonfiore della lingua, le labbra e le labbra), gli orticaria o l'eruzione cutanea, devono essere immediatamente arrestati e un trattamento alternativo deve essere stabilito.
paradossale
Come per qualsiasi farmaco somministrato per via inalata, la somministrazione di questo farmaco può portare a un broncospasmo paradossale che può iniziare la prognosi vitale. In caso di broncospasmo paradossale, il trattamento deve essere immediatamente interrotto e deve essere stabilito un trattamento alternativo.
Effetti pronti dei beta-agonisti
Come altri farmaci contenenti agonisti beta-2-adrenergici, questo farmaco può indurre in alcuni pazienti significativi, con conseguente aumento della frequenza cardiaca, della pressione arteriosa e/o dei sintomi. Se si verificano tali effetti, potrebbe essere necessario interrompere il trattamento.
Questo farmaco dovrebbe essere usato con cautela nei pazienti con condizioni cardiovascolari (coronaropatia, infarto miocardico acuto, aritmie cardiache, ipertensione), storia di convulsione o tireotossicosi e nei pazienti con idiosincratico a beta-2-agonisti.
Les patients ayant un angor instable, un antécédent d'infarctus du myocarde au cours des 12 derniers mois, une insuffisance ventriculaire gauche de classe NYHA III/IV (New York Heart Association), une arythmie, une hypertension non contrôlée, une maladie cérébrovasculaire ou un antécédent de syndrome du QT long et les patients traités par des médicaments connus pour allonger l'intervalle QTc ont été exclus des études du programme de développement clinique d'indacatérol/furoate de mométasone. Par conséquent, les données en matière de sécurité d'emploi dans ces populations sont considérées comme inconnues.
Si des modifications de l'électrocardiogramme (ECG) telles qu'un aplatissement de l'onde T, un allongement de l'intervalle QT et un sous-décalage du segment ST ont été rapportées avec les bêta-2-agonistes, la pertinence clinique de ces observations est inconnue.
Les bêta 2 agonistes de longue durée d'action (LABA) ou les associations de substances actives contenant des LABA telles que Atectura Breezhaler doivent par conséquent être utilisés avec prudence chez les patients dont l'allongement de l'intervalle QT est connu ou suspecté ou chez les patients traités par des médicaments ayant un effet sur l'intervalle QT.
Iponokalemia con beta-agonisti
Les bêta-2-agonistes peuvent induire chez certains patients une hypokaliémie significative, pouvant entraîner des effets indésirables cardiovasculaires. La diminution de la kaliémie est généralement transitoire et ne nécessite pas de supplémentation. Chez les patients présentant un asthme sévère, les effets hypokaliémiants peuvent être potentialisés par l'hypoxie et par des traitements concomitants, ce qui peut accroître la prédisposition au risque d'arythmies cardiaques (voir rubrique interazioni). L'ipokalemia non è stata osservata negli studi clinici sull'inadaterolo/Mometasone furoato alla dose terapeutica raccomandata.
Aucun cas cliniquement pertinent d'hypokaliémie n'a été observé dans les études cliniques de l'indacatérol/furoate de mométasone à la dose thérapeutique recommandée.
iperglicemia
L'inalazione di alte dosi di beta-2-agonisti e corticosteroidi può indurre aumenti di zucchero nel sangue. La glicemia deve essere monitorata più da vicino nei pazienti diabetici non appena viene stabilito il trattamento.
Ce médicament n'a pas été étudié chez les patients présentant un diabète de type I ou un diabète de type II insuffisamment contrôlé.
= Prevenzione delle infezioni orofaringee
Afin de réduire le risque d'infection oropharyngée à candida, il faut recommander aux patients de se rincer la bouche ou de se gargariser avec de l'eau sans l'avaler ou de se brosser les dents après l'inhalation de chaque dose.
Effetti sistemici collegati alla terapia corticosteroide
Gli effetti sistemici legati ai corticosteroidi inalati possono verificarsi, in particolare durante il trattamento a lungo termine. Questi effetti hanno molto meno probabilità che si verifichino rispetto alla terapia corticosteroide orale e gli effetti possono variare da un paziente all'altro e secondo le diverse preparazioni di corticosteroidi.
= I possibili effetti sistemici possono includere una sindrome di Cushing, manifestazioni di cushingoidi, un'inibizione della funzione surrenale, un ritardo di crescita nei bambini e adolescenti, una diminuzione della densità minerale ossea, della cataratta, del glaucoma e del depressioni (in particolare dei bambini in ansia, dell'ansia, dell'ansia, dell'ansia, della depressione del sonno). È quindi importante che la dose di corticosteroidi inalati sia regolata alla dose più bassa con cui viene mantenuto un controllo efficace dell'asma.
Disturbi visivi possono essere riportati con l'uso di corticosteroidi sistemici e topici (inclusi intranasali, inalati e intraoculari). I pazienti con sintomi come una visione travagliata o altri disturbi visivi, devono essere orientati verso un oftalmologo per una valutazione delle possibili cause dei disturbi visivi, che possono includere cataratta, glaucoma o malattie rare come la coritinopatia sereosa centrale (CSCR) che è stata riportata dopo l'uso di corticosterie sistemiche e topico.
Questo farmaco deve essere somministrato con cautela nei pazienti con tubercolosi polmonare o in pazienti con infezioni croniche o non trattate.
EXPIPIENTS
Questo farmaco contiene lattosio. I pazienti con intolleranza al galattosio, deficit di lattasi totale o sindrome da malassorbimento di glucosio e galattosio (malattie ereditarie rare) non dovrebbero assumere questo medicinale.
interazioni |
Connect per accedere a questo contenuto
Fertilità/Gravidanza/Affetto al seno |
gravidanza
I dati relativi all'uso di atectura breezhaler o dei suoi singoli componenti (indicaterolo e mumétasone furoate) nelle donne in gravidanza non sono sufficienti per determinare se esiste un rischio.
L'Idacateroce non è stato teratogenico nei ratti e nel coniglio dopo il percorso sottocutaneo (vedere SezioneSécurité préclinique). Negli studi di riproduzione su topi, ratti e conigli incinti, il mometasone furoato ha aumentato le malformazioni fetali e ridotto la sopravvivenza e la crescita del feto.
Comme les autres médicaments contenant des agonistes bêta-2-adrénergiques, l'indacatérol peut inhiber le travail au moment de l'accouchement par effet relaxant sur le muscle lisse utérin.
Questo farmaco dovrebbe essere utilizzato durante la gravidanza solo se il beneficio atteso per il paziente giustifica il potenziale rischio per il feto.
allattamento al seno
Non ci sono dati disponibili sulla presenza di indicaterolo o mometasone nel latte materno o sugli effetti sulla produzione di latte. Altri corticosteroidi inalati simili al passaggio del mometasone attraverso il latte materno. L'inacaterolo (compresi i suoi metaboliti) e l'ebollizione del mumetasone sono stati rilevati nel latte materno.
Une décision doit être prise soit d'interrompre l'allaitement soit d'interrompre/de s'abstenir du traitement en prenant en compte le bénéfice de l'allaitement pour l'enfant au regard du bénéfice du traitement pour la femme.
Fertilità
Gli studi riproduttivi e gli altri dati negli animali non indicano alcun effetto avverso sulla fertilità nei maschi o nelle femmine.
guida e utilizzo di macchine |
Questo medicinale non ha alcun effetto o effetto trascurabile sulla capacità di guidare veicoli e utilizzare macchine.
EFFETS INDÉSIRABLES |
Connect per accedere a questo contenuto
Overdose |
una sorveglianza e un trattamento sintomatico sono raccomandati in caso di sovradosaggio.
ourrdosage dovrebbe probabilmente portare a segni, sintomi o effetti indesiderati associati agli individui (ad esempio tachicardia, tremori, palpitazioni, mal di testa, nausea, vomito, sonnolenza, aritmie ventricolari-surdiante, acido metabolico, acidosi metabolica, ipokalemia, iperglicemia, inibizione dell'ipotalamo-sussisa). | Cardioselettivo può essere considerato per il trattamento degli effetti beta-2-adrenergici, ma solo sotto la supervisione di un medico e con estrema cautela perché la somministrazione di beta-bloccanti può indurre un broncospasmo. In casi gravi, i pazienti devono essere ricoverati in ospedale.
L'utilisation de bêta-bloquants cardiosélectifs peut être envisagée pour traiter les effets bêta-2-adrénergiques, mais uniquement sous la surveillance d'un médecin et avec une extrême prudence car l'administration de bêta-bloquants peut induire un bronchospasme. Dans les cas graves, les patients doivent être hospitalisés.
Farmacodinamica |
Connettiti per accedere a questo contenuto
Pharmacokinetics |
Connettiti per accedere a questo contenuto
Preclinical |
Associazione di INDACATEROL e MEMETASONE FUROATE
Le osservazioni fatte durante gli studi di tossicità da una via inalatoria di 13 settimane sono principalmente attribuibili al componente feroato di Mometasone e corrispondono agli effetti farmacologici caratteristici dei glucocorticoidi. Gli aumenti della frequenza cardiaca associati all'inacaterolo sono stati osservati nei cani dopo la somministrazione di indicaterolo/mometasone solaoato o indecaterolo da solo.
INDACATEROL
Nei cani, gli effetti sul sistema cardiovascolare attribuibili ai beta-2-agonisti dell'inacaterolo erano tachicardia, aritmia e lesioni miocardiche. Una leggera irritazione della cavità nasale e della laringe è stata osservata nei roditori.
Studi di genotossicità non hanno rivelato mutagene o potenziale clastogenico.
La carcinogenicità è stata valutata in uno studio di due anni nei ratti e in uno studio di sei mesi in un topo transgenico. Le maggiori implicazioni dei leiomiomi ovarici benigni e l'iperplasia focale del muscolo ovaio liscio nella femmina mancante con le osservazioni simili riportate per altri agonisti di adrenergici beta-2. Non è stato osservato alcun segno di cancerogenicità nei topi.
Tutti questi effetti si sono verificati in mostre molto più alte di quelle previste nell'uomo.
Après administration sous-cutanée dans une étude chez le lapin, les effets indésirables de l'indacatérol sur la grossesse et le développement embryo-fœtal n'ont été observés qu'à des doses plus de 500 fois supérieures à celles obtenues après l'inhalation quotidienne de 150 mcg chez l'homme (sur la base de l'ASC0-24 h).
Bien que l'indacatérol n'ait pas affecté les fonctions de reproduction générales dans une étude de fertilité chez le rat, une diminution du nombre de femelles rat gravides à la génération F1 a été observée lors d'une étude du développement péri- et post-natal chez le rat à une exposition 14 fois plus élevée que celle observée chez l'homme lors du traitement par l'indacatérol. L'indacatérol n'a pas été embryotoxique ou tératogène chez le rat ou le lapin.
Mometasone furoate
Tutti gli effetti osservati sono caratteristici della classe di glucocorticoidi e corrispondono a un'esacerbazione degli effetti farmacologici dei glucocorticoidi. | De Mometasone non ha mostrato alcuna attività genotossica in una batteria di test standard di test
Le furoate de mométasone n'a pas montré d'activité génotoxique dans une batterie standard de tests in vitro e in vivo.
In studi di cancerogenicità su topi e ratto, mumeta di aumento statisticamente significativo dell'incidenza dei tumori.
Comme les autres glucocorticoïdes, le furoate de mométasone est tératogène chez les rongeurs et les lapins. Les effets observés ont été l'apparition de hernies ombilicales chez le rat, de fentes palatines chez la souris et d'agénésies de la vésicule biliaire, de hernies ombilicales et de flexions des pattes avant chez le lapin. Il a également été observé une baisse de la prise de poids chez les mères, des effets sur la croissance fœtale (poids fœtal plus faible et/ou retard d'ossification) chez le rat, le lapin et la souris, de même qu'une diminution de la survie de la progéniture chez la souris. Dans les études sur la fonction de reproduction, l'injection sous-cutanée de furoate de mométasone, à la dose de 15 mcg/kg, a entraîné un allongement de la gestation ainsi qu'un accouchement difficile avec une réduction de la survie et du poids de la progéniture.
Valutazione del rischio ambientale
Des études d'évaluation du risque environnemental ont montré que la mométasone peut présenter un risque pour les eaux de surface (voir rubrique Eliminazione/Manipolazione).
ufficiale di conservazione |
3 anni.
PRECAUZIONI DELLA CONSERVAZIONE |
30 ° C.
da conservare nella confezione originale riparata dalla luce e dall'umidità.
Precauzioni per l'eliminazione e la manipolazione |
È consigliabile utilizzare l'inalatore fornito con ogni nuova prescrizione. L'inalatore incluso in ogni scatola deve essere eliminato dopo che tutte le capsule di questa scatola sono state utilizzate.
Questo farmaco può presentare un rischio per l'ambiente (vedere la sezione Sicurezza preclina).
Qualsiasi droga o rifiuti non utilizzati deve essere eliminato in conformità con l'uso e la manipolazione dei regolamenti
Instructions pour l'utilisation et la manipulation
Lire l'ensemble des Istruzioni per la manipolazione prima di usare Atectura Breezhaler.
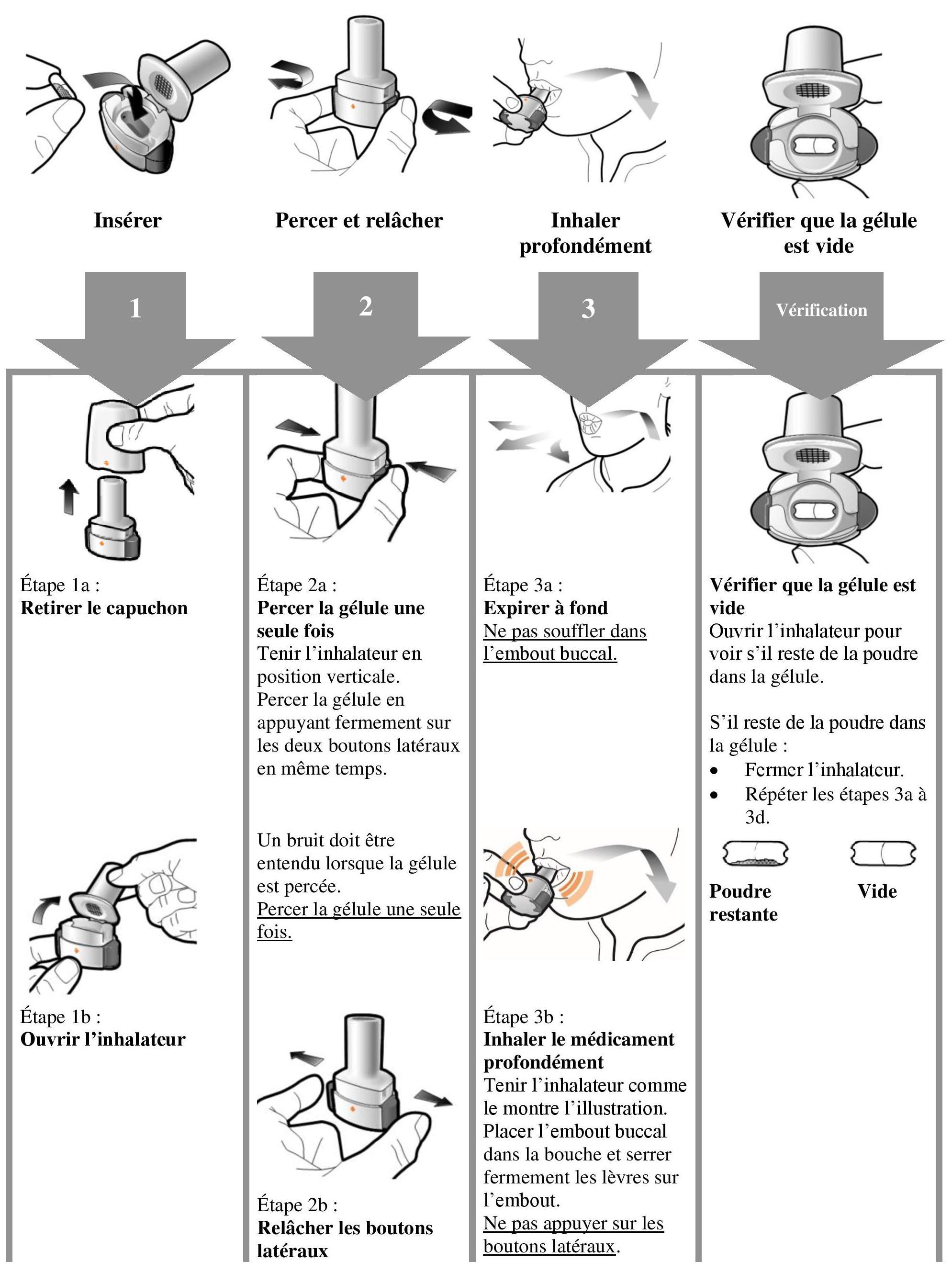
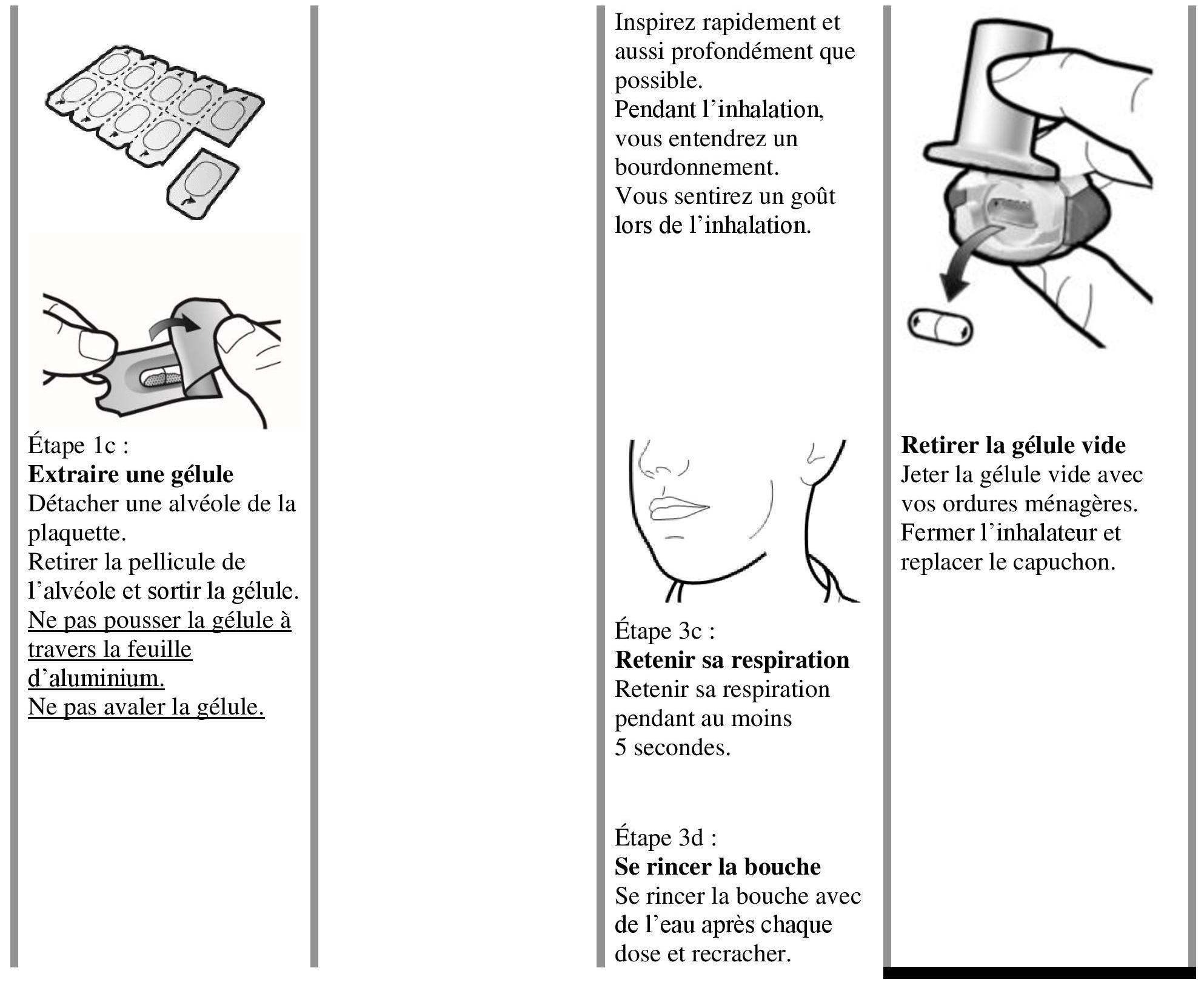
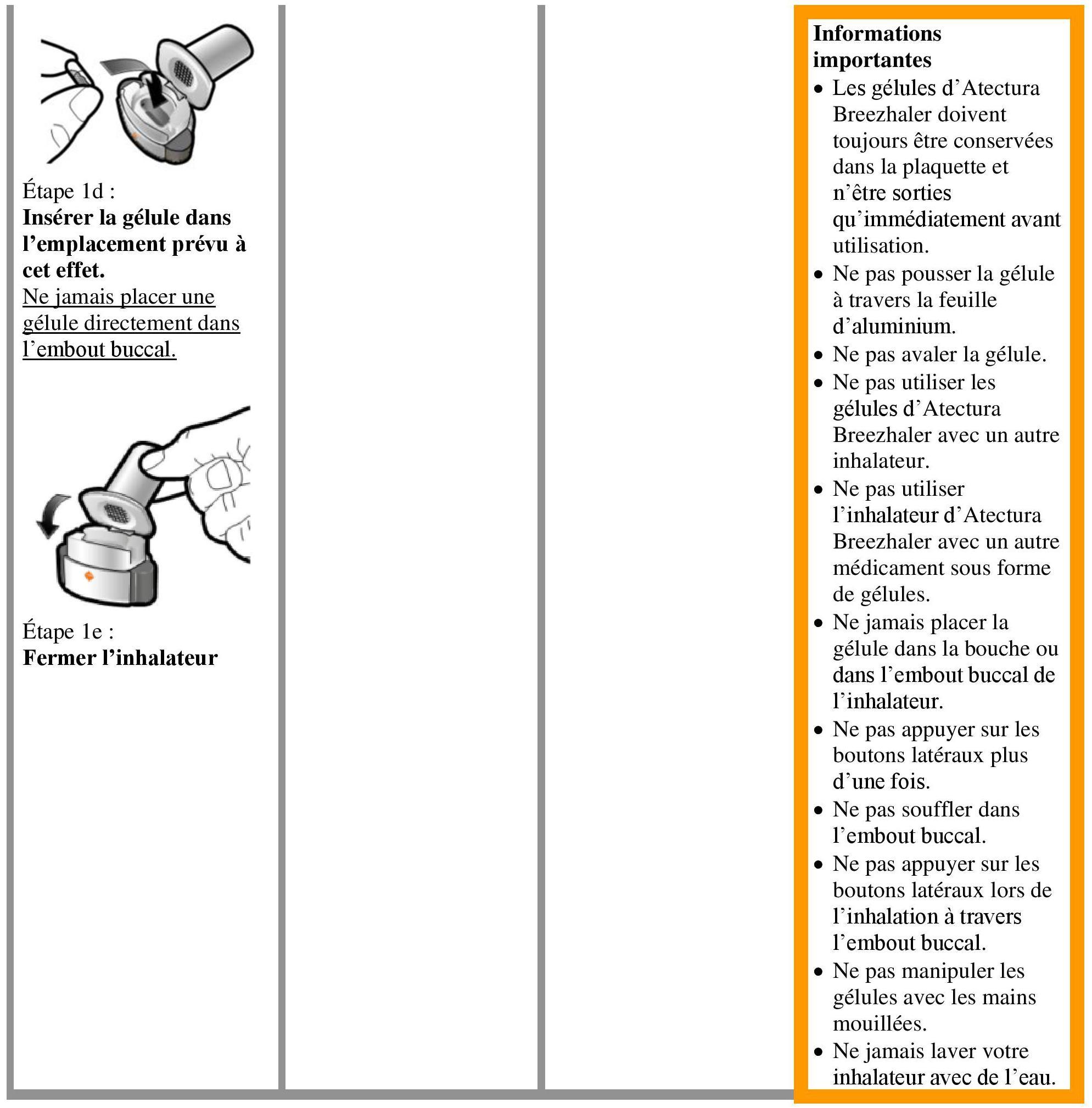

prescrizione/consegna/sviluppo |
| AMM |
|
| Prezzo: |
|
| AMM |
|
| Prezzo: |
|
| AMM |
|
| Prezzo: |
|
REMB SEC SOC al 65%. Raccogliere.
Modello ospedaliero: raccolta.
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l'Agence européenne des médicaments : https: //www.ema.europa.eu. | The AMM:
Titulaire de l'AMM : Novartis European Limited, Vista Building, Elm Park, Merrion Road, Dublino 4, Irland.
 = Documento utile Vidal
= Documento utile Vidal